CO43923 ist eine Plattformstudie, in der die Sicherheit und Wirksamkeit verschiedener Behandlungen als Monotherapie oder als Kombinationstherapie bei Teilnehmern mit Multiplem Myelom (MM) untersucht werden. Außerdem wird erforscht, wie die Arzneimittel im Körper verarbeitet werden (Pharmakokinetik). Die Studie ist so konzipiert, dass Teilstudien zu neuen Behandlungen hinzugefügt werden können, sobald diese verfügbar sind. Informationen zu den begonnenen Teilstudien finden Sie weiter unten.
Organisatorische Daten:
| Prüfplancode: | CO43923 |
| EudraCt | 2021-005918-34 |
| EU CT: | 2023-504484-16-00 |
| Clinicaltrials.gov: | NCT05583617 |
| DRKS: | |
| Sponsor: | Hoffmann La Roche |
| Studienphase: | Phase 1/2 |
| Status: | Rekrutierung läuft, geplant bis Mai 2027 |
Hauptstudie (PLYCOM):
- in dieser Studie wird die Sicherheit der Studienbehandlung bewertet. Zudem wird auch die Verträglichkeit und der Dosierungsschemen und der Dosen untersucht.
Teilstudie 2 (DIRAC): Cevostamab + Lenalidomid
- Diese Teilstudie untersucht die Kombination von Cevostamab und Lenalidomid als Erhaltungstherapie nach einer Transplantation bei Teilnehmern mit MM mit zytogenetischen Hochrisikomerkmalen, die nach der Induktion mindestens ein partielles Ansprechen erreicht haben.
Teilstudie 4 (CHWLA): Cevostamab + Iberdomid
- Diese Teilstudie untersucht die Sicherheit, Verträglichkeit, Pharmakokinetik (Verarbeitung des Arzneimittels durch den Körper) und Pharmakodynamik (Wirkungen des Arzneimittels auf den Körper) der Kombination von Cevostamab und Iberdomid bei Teilnehmern mit rezidiviertem oder refraktärem MM. Teilnehmer in dieser Teilstudie haben mindestens drei vorherige Therapielinien erhalten, darunter einen Proteasom-Inhibitor (PI), einen monoklonalen Anti-CD38-Antikörper und einen immunmodulatorischen Wirkstoff (IMiD).
Hintergrund:
Cevostamab ist ein Antikörper, der gegen zwei Ziele gerichtet (bispezifisch) ist: gegen das sogenannte Fc-Rezeptor-Homolog 5 (FcRH5) und gegen CD3. FcRH5 wird ausschließlich auf B-Zellen exprimiert und kommt auf den meisten MM-Zellen vor. CD3 ist an der Aktivierung der Immunantwort zur Bekämpfung von Infektionen beteiligt.
Durchführung:
Teilstudie 2 (DIRAC):
- In der Vorphase erhalten die Teilnehmer zwei steigende Dosen und eine Zieldosis von Cevostamab als intravenöse Infusion. Lenalidomid wird oral verabreicht.
Teilstudie 4 (CHAWLA):
- In der Vorphase erhalten die Teilnehmer zwei steigende Dosen und eine Zieldosis von Cevostamab als intravenöse Infusion. Iberdomid wird oral verabreicht.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
Einschlusskriterien für die Hauptstudie:
- Diagnose eines MM gemäß den Kriterien der International Myeloma Working Group (IMWG)
- Leistungsstatus gemäß Eastern Cooperative Oncology Group Performance Status (ECOG, Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0, 1 oder 2
- Auflösung von unerwünschten Ereignissen aus einer früheren Krebstherapie auf Grad 0 oder 1
- Zustimmung zur Teilnahme an geplanten Untersuchungen und Verfahren
Zusätzliche Einschlusskriterien für Teilstudie 2:
- Abschluss einer geplanten Induktionstherapie und Erreichen mindestens eines partiellen Ansprechens
- Autologe Stammzelltransplantation innerhalb von 100 Tagen vor der ersten Studienbehandlung und Fehlen einer fortschreitenden Erkrankung
- Vorliegen von zytogenetischen Hochrisikomerkmalen bei der Diagnosestellung
Zusätzliche Einschlusskriterien für Teilstudie 4:
- Patienten mit rezidiviertem/refraktärem MM, die eine Vorbehandlung mit mindestens einem PI, einem IMiD und einem Anti-CD38-Antikörper erhalten haben und für die keine geeignete Standardtherapieoptionen verfügbar sind
Ausschlusskriterien:
- Unfähigkeit, die im Protokoll vorgeschriebenen Krankenhausaufenthalte und Verfahren einzuhalten
- Vorgeschichte einer bestätigten progressiven multifokalen Leukoenzephalopathie
- Vorgeschichte anderer bösartigen Erkrankung innerhalb von 2 Jahren vor der Voruntersuchung
- Aktuelle oder frühere Erkrankung des Zentralnervensystems (ZNS)
- Schwere Herz-Kreislauf-Erkrankung
- Symptomatische aktive Lungenerkrankung oder Notwendigkeit einer zusätzlichen Sauerstoffversorgung
Zusätzliche Ausschlusskriterien für Teilstudie 2:
- Überempfindlichkeitsreaktionen gegenüber Lenalidomid oder anderen immunmodulierenden Arzneimitteln
- Schädigungen in der Nähe von lebenswichtigen Organen, die bei einem Aufflammen der Tumorerkrankung zu einer plötzlichen Entgleisung/Verschlechterung führen können
- Vorbehandlung mit einem Prüfmedikament, einer systemischen Krebstherapie oder Immuntherapien in einem Arm der Studie CO43923 innerhalb von 5 Halbwertszeiten oder 3 Wochen, je nachdem, was kürzer ist
- Bekannte aktive bakterielle, virale, pilzbedingte, mykobakterielle, parasitäre oder sonstige Infektion (mit Ausnahme von Pilzinfektionen des Nagelbetts) bei Studieneinschluss oder jede schwerwiegende Infektion, die eine Behandlung mit intravenösen antimikrobiellen Arzneimitteln erforderte, wobei die letzte Dosis des intravenösen antimikrobiellen Arzneimittels innerhalb von 14 Tagen vor der ersten Studienbehandlung verabreicht wurde.
- Vorgeschichte eines Erythema multiforme von Grad 3 oder höher oder Blasenbildung nach Vorbehandlung mit immunmodulierenden Substanzen
Zusätzliche Ausschlusskriterien für Teilstudie 4:
- Behandlung mit Prüfmedikamenten, systemischen Krebstherapien, Immuntherapien innerhalb von 5 Halbwertszeiten oder 12 Wochen vor Beginn der Vorphase
- Vorgeschichte einer Anaphylaxie oder Überempfindlichkeit, einschließlich eines Hautausschlags von Grad 3 oder höher, während der Vorbehandlung mit IMiDs, Dexamethason, etwaigen Cereblon-E3-Ligase-Modulatoren (CELMoDs), oder gegen über den in den Arzneimitteln enthaltenen Bestandteilen
- Bekannte Anaphylaxie, Allergien, Überempfindlichkeit oder Unverträglichkeit gegenüber bestimmten Substanzen oder Proteinen, wie im Prüfplan definiert
- Verabreichung starker CYP3A-Modulatoren, Verabreichung von Protonenpumpenhemmern innerhalb von 2 Wochen nach Beginn der Studienbehandlung
- Unkontrollierter Bluthochdruck oder unkontrollierter Diabetes innerhalb von 14 Tagen vor Studieneinschluss
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt
Iberdomid vs. Iberdomid plus Isatuximab Erhaltungstherapie nach ASCT bei neu diagnostiziertem Multiplem Myelom
Organisatorische Daten:
| Prüfplancode: | GMMG-HD 9 /
DSMM XVIII |
| ISRCTN: | |
| EUCT | 2023-507402-13-00 |
| Clinicaltrials.gov: | |
| DRKS: | |
| Sponsor: | Universitätsklinikum Heidelberg DSMM, |
| Studienphase: | |
| Status: | Rekrutierung geplant bis Juni 2026 |
Ziel:
Ziel dieser klinischen Studie ist es, eine Erhaltungstherapie aus Iberdomid und Isatuximab mit einer reinen Iberdomid-Therapie zu vergleichen. Die Studie ist die Folgestudie zur Erhaltungstherapie der GMMG-HD8/DSMM XIX-Studie für Patienten mit neu diagnostiziertem multiplem Myelom. Patienten mit neu diagnostiziertem Multiplem Myelom, die ein ähnliches Behandlungsschema mit einer Induktions-/
Durchführung:
Die Randomisierung wird zentral von den GMMG/DSMM-Büros durchgeführt, nachdem die Eignung der Patienten überprüft wurde. Zum Zeitpunkt des Studieneinschlusses erfolgt die Randomisierung in Arm A (Iberdomid) oder Arm B (Iberdomid + Isatuximab). Die Randomisierung erfolgt stratifiziert nach dem zentral bewerteten MRD-Negativitätsstatus (ja vs. nein vs. unbekannt; bewertet durch NGF von BMA; Sensitivität von 10^-5; unabhängig von der Standard-IMWG-Antwort) und der Anzahl der HDM/ASCT (einfach vs. tandem).
Die in Arm A randomisierten Patienten erhalten 39 Zyklen des Medikaments Iberdomid, ein Cereblon E3 Ubiquitin Ligase Modulating Drug (CELMoD®), das strukturelle Ähnlichkeiten mit den immunmodulatorischen Substanzen (IMiDs) wie Thalidomid und Lenalidomid aufweist. Jeder Zyklus wird 29 Tage dauern. Die Patienten in Arm B erhalten dieselben 39 Zyklen von Iberdomid plus dem monoklonalen Anti-CD38-Antikörper Isatuximab subkutan. In beiden Armen erhalten die Patienten im Zyklus 1 20 mg Dexamethason, und zwar an denselben Tagen wie die Verabreichung von Isatuximab in Arm B. Das Ende der Studie ist nach 36 Monaten der Erhaltungstherapie.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Vorherige Aufnahme und Behandlung im Rahmen der GMMG-HD8 / DSMM XIX-Studie ODER
- Erstlinien-Vierfach-
Induktionstherapie, ggf. einschließlich einer Konsolidierung, bestehend aus einem Proteasom-Inhibitor, einem Immunmodulator, Dexamethason (oder einem gleichwertigen Wirkstoff) und einem anti-CD38-Antikörper
- Eine Konsolidierung nach Hochdosistherapie mit Melphalan/autologer Stammzelltransplantation, die ähnliche Substanzen enthält wie die Induktionstherapie, ist erlaubt.
- Die Induktions- und ggf. Konsolidierungstherapie sollte insgesamt mindestens 4 und maximal 6 Zyklen dauern. Die Konsolidierungstherapie darf maximal 2 Zyklen nach Hochdosistherapie mit Melphalan/autologer Stammzelltransplantation umfassen. UND - Erhalt mindestens ein Zyklus Hochdosis-Melphalan-Therapie (HDM) und autologe Stammzelltransplantation (ASCT) erhalten
- Mindestens partielles Ansprechen (PR) nach den IMWG-Kriterien bei Aufnahme in die Studie
- Alter von mindestens 18 Jahren bei StudieneinschlussWHO-Leistungsstatus von 0, 1 oder 2
- Negativer Schwangerschaftstest bei Studieneinschluss (Frauen im gebärfähigen Alter)
-
Ausschlußkriterien:
- Patienten mit Magen-Darm-Erkrankungen, die die Resorption von Iberdomid erheblich beeinträchtigen können
- Patienten mit bekannter Überempfindlichkeit (oder Kontraindikation) gegen einen der Bestandteile der Studientherapie, die nicht mit Steroiden oder H1-Blockern prämediziert werden können und die eine weitere Behandlung mit diesen Mitteln verbieten würden (z. B. bekannte Unverträglichkeit oder Überempfindlichkeit gegen infundierte Eiweißprodukte, Saccharose, Histidin und Polysorbat 80 sowie Unverträglichkeit gegen Arginin und Poloxamer 188)
- Patienten mit einer schweren allergischen Reaktion auf einen anderen immunmodulatorischen Wirkstoff (Thalidomid, Lenalidomid oder Pomalidomid) in der Vorgeschichte", wie Angioödem und schwere dermatologische Reaktionen, einschließlich Hautausschlag des Grades 4 und exfoliativen oder bullösen Hautausschlag
- Patienten, die derzeit mit starken Inhibitoren oder Induktoren von CYP3A4/5 behandelt werden
- Systemische AL-Amyloidose (außer lokalisierte AL-Amyloidose, die auf die Haut oder das Knochenmark beschränkt ist), Plasmazellleukämie oder Polyneuropathie, Organomegalie, Endokrinopathie, monoklonale Protein- und Hautanomalien oder Waldenström-Makroglobulinämie.
- Vorherige systemische Anti-Myelom-Behandlung, die nicht im Rahmen der GMMG-HD8 / DSMM XIX-Studie verabreicht oder nicht in den oben genannten Einschlusskriterien definiert wurde (einschließlich bis zu zwei Zyklen hochdosierter Melphalan-Therapie und aurologer Stammzelltransplantation)
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Teclistamab, Daratumumab, Lenalidomid,Dexamethason +/- Bortezomib
Phase-2-Studie zur Bewertung der Sicherheit und Wirksamkeit von Teclistamab in Kombination mit Daratumumab, Lenalidomid und Dexamethason mit und ohne Bortezomib als Induktionstherapie und Teclistamab in Kombination mit Daratumumab und Lenalidomid als Erhaltungstherapie bei transplantationsgeeigneten Patienten mit neu diagnostiziertem Multiplem Myelom
Organisatorische Daten:
| Prüfplancode: | GMMG-HD10, DSMM-XX, 64007957MMY2003, MajesTEC-5 |
| ISRCTN: | |
| EudraCT: | |
| Clinicaltrials.gov: | NCT05695508 |
| DRKS: | |
| Sponsor: | Universitätsklinikum Heidelberg in Zusammenarbeit mit Janssen |
| Studienphase: | Phase 3 |
| Status: | Rekrutierung läuft, geplant bis Mai 2026 |
Hintergrund:
Teclistamab ist ein bispezifischer Antikörper, der an das B-Zell-Reifungsantigen (BCMA), ein Protein auf der Oberfläche von Myelomzellen, bindet und gegen CD3-Rezeptoren auf der Oberfläche von T-Zellen gerichtet ist. Teclistamab wurde im August 2022 in der EU als Monotherapie zur Behandlung des fortgeschrittenen Multiplen Myeloms zugelassen und wird jetzt bei weiteren Indikationen geprüft.
In dieser Studie bei Patienten mit neu diagnostiziertem Multiplem Myelom, die für eine Transplantation geeignet sind, werden die Sicherheit, Verträglichkeit und Wirksamkeit einer Fünffach-Kombination in der Induktionstherapie geprüft: Teclistamab (Tec) in Kombination mit Daratumumab (Dara), Lenalidomid (R), Bortezomib (V) und Dexamethason (d).
Durchführung
Das Studiendesign gliedert sich in drei Studienarme:
Patienten in Arm A und B erhalten eine Induktionstherapie mit Tec-Dara-Rd (Arm A) oder Tec-Dara-VRd (Arm B). Es folgen eine Hochdosis-Chemotherapie und eine autologe Stammzelltransplantation gemäß Therapiestandard sowie eine Erhaltungstherapie mit Tec-Dara-R.
Patienten in Arm C erhalten eine Induktionstherapie gemäß Therapiestandard gefolgt von einer Hochdosis-Chemotherapie und einer autologen Stammzelltransplantation sowie gegebenenfalls einer Konsolidierungstherapie. Im Anschluss daran folgt eine Erhaltungstherapie mit Tec-Dara-R.
Die Behandlungsdauer der Induktionsphase beträgt 6 Zyklen (à 28 Tage). Im Anschluss daran folgen eine Hochdosis-Chemotherapie und autologe Stammzelltransplantation . Danach beginnt die Erhaltungsphase der Studie unter Tec-Dara-R über 18 Zyklen.
Studienarm C beginnt mit dem Screening nach abgeschlossener Hochdosis-Chemotherapieplus autologer Stammzelltransplantation. Die Behandlung erfolgt genauso wie in Arm A und B mit Tec-Dara-R als Erhaltungstherapie für 18 Zyklen.
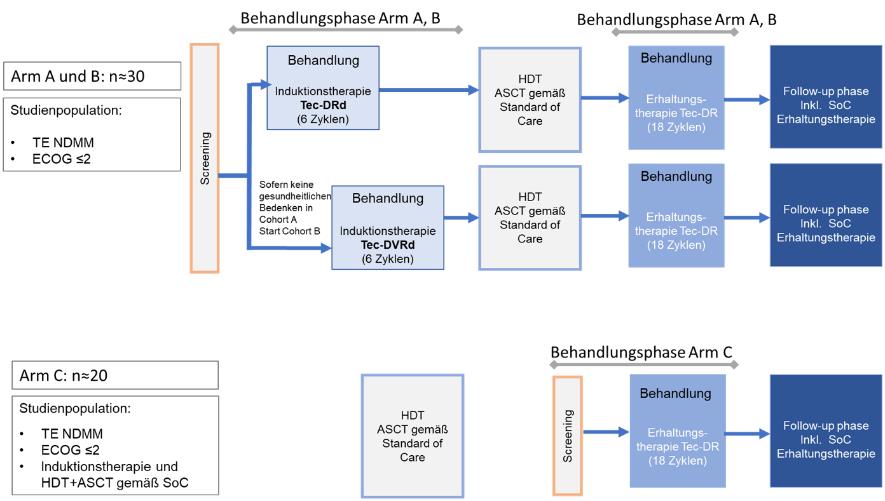
Abb. Studiendesign, mit freundlicher Genehmigung des Universitätsklinikums Heidelberg, Prof. Raab
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Neu diagnostiziertes Multiples Myelom gemäß den Diagnosekriterien der International Myeloma Working Group (IMWG) und Erhalt einer Induktionstherapie mit oder ohne Konsolidierung
- Ein ECOG-Performance-Status-Score (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0, 1 oder 2 beim Screening und unmittelbar vor Beginn der Verabreichung der Studienbehandlung
- Messbare Erkrankung während der Screening-Phase, gemäß der Definition im Protokoll
Ausschlusskriterien
- Beteiligung des ZNS oder klinische Anzeichen für eine Beteiligung der Hirnhäute
- Schlaganfall oder Krampfanfall innerhalb von 6 Monaten vor Studienbeginn
- Transplantation in der Krankengeschichte, die eine immunsuppressive Behandlung erforderte
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Phase 3- Studie zu Teclistamab
Eine Studie zu Teclistamab in Kombination mit Lenalidomid und Teclistamab allein im Vergleich zu Lenalidomid allein bei Teilnehmern mit neu diagnostiziertem Multiplem Myelom als Erhaltungstherapie nach autologer Stammzelltransplantation (MajesTEC-4)
Organisatorische Daten:
| Prüfplancode: | EMN30/64007957MMY3003 |
| ISRCTN: | |
| EudraCT: | |
| Clinicaltrials.gov: | NCT05243797 |
| DRKS: | |
| Sponsor: | JEuropean Myeloma Network B.V in ZUsammenarbeit mit Janssen Pharmaceutica |
| Studienphase: | Phase 3 |
| Status: | Rekrutierung läuft, geplant bis Oktober 2028 |
Ziele:
Ziel dieser Studie ist es, den Nutzen von Teclistamab in Kombination mit Lenalidomid und von Teclistamab als Monotherapie im Vergleich zu einer Monotherapie mit Lenalidomid bei Patienten mit Multiplem Myelom nach einer autologen Stammzelltherapie zu überprüfen.
Hintergrund:
Teclistamab ist ein bispezifischer Antikörper, der sowohl gegen das B-Zell-Reifungsantigen (BCMA), ein Protein auf Myelomzellen, als auch gegen CD3-Rezeptoren auf der T-Zell-Oberfläche gerichtet ist. Teclistamab wurde im August 2022 in der EU als Monotherapie zur Behandlung des fortgeschrittenen Multiplen Myeloms zugelassen und wird jetzt bei weiteren Indikationen geprüft.
In der MajesTEC-1-Studie bei stark vorbehandelten Patienten mit Multiplem Myelom (n=165) bewirkte Teclistamab ein hohes und dauerhaftes Ansprechen. Bei einer medianen Nachbeobachtungszeit von etwa 14 Monaten betrug die Gesamtansprechrate 63 Prozent, wobei 39,4 Prozent ein komplettes Ansprechen oder besser erreichten. Diese Daten wurden auf der Jahrestagung 2022 der American Society of Clinical Oncology (ASCO) veröffentlicht.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Neu diagnostiziertes Multiples Myelom gemäß den Diagnosekriterien der International Myeloma Working Group (IMWG) und Erhalt einer Induktionstherapie mit oder ohne Konsolidierung
- Erhalt nur einer Therapielinie und Erreichen eines mindestens partiellen Ansprechens gemäß den IMWG-Ansprechkriterien ohne Anzeichen einer Progression zum Zeitpunkt der ersten Gabe der Studienmedikation
- ECOG-Performance-Status-Score (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0, 1 oder 2 beim Screening und unmittelbar vor Beginn der Verabreichung der Studienmedikation
Ausschlusskriterien:
- Unverträglichkeit gegenüber der Anfangsdosis von Lenalidomid
- Erhaltungstherapie
- Vorherige gegen das B-Zell-Reifungsantigen (BCMA) gerichtete Therapie
- Vorherige Therapie mit einem Mittel, das Immunzellen neu ausrichtet, oder einer gentechnisch veränderten adoptiven Zelltherapie (z. B. mit chimärem Antigenrezeptor-modifizierte T-Zellen, NK-Zellen)
- Abbruch der Behandlung aufgrund einer Nebenwirkung von Lenalidomid, bei der der Prüfarzt einen Zusammenhang mit Lenalidomid sieht
- Fortschreiten des Multiplen Myeloms zu irgendeinem Zeitpunkt vor dem Screening
- Erhalt einer kumulativen Kortikosteroid-Dosis, die ≥ 140 mg Prednison entspricht, in den 14 Tagen vor der ersten Behandlungsdosis
- Impfung mit einem abgeschwächten Lebendimpfstoff innerhalb von 4 Wochen vor der ersten Behandlungsdosis. Totimpfstoffe und nicht replizierende, für den Notfall zugelassene Impfstoffe sind erlaubt.
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt
Ein neuer Cereblon E3 Ligase Modulator
Eine Studie zur Bestimmung der empfohlenen Dosis und des Regimes und zur Bewertung der Sicherheit und vorläufigen Wirksamkeit von CC-92480 in Kombination mit Standardbehandlungen bei Patienten mit rezidiviertem oder refraktärem Multiplen Myelom (RRMM) und neu diagnostiziertem Multiplen Myelom (NDMM)
Organisatorische Daten:
| Prüfplancode: | CC-92480-mm-02 |
| UTMS | U1111-1233-5619 |
| EudraCT: | 2018-004767-31 |
| Clinicaltrials.gov: | NCT03989414 |
| DRKS: | |
| Sponsor: | Celgene |
| Studienphase: | Phase 1/2 |
| Status: | Rekrutierung läuft, geplant bis Januar 2025 |
Hintergrund:
CC-92480 ist ein sogenannter CRBN-Modulator [Cereblon-(CRBN-)E3-Ligase-Modulator (CELMoD)]. Dieser neuartige Modulator hat vielfältige Wirkungen und wirkt unter anderem stark immunmodulierend. Der Wirkstoff führt zu einem schnellen, tiefen und anhaltenden Zerfall von Ikaros und Aiolos – zwei Faktoren, die zum Überleben der Myelomzellen beitragen.
Durchführung:
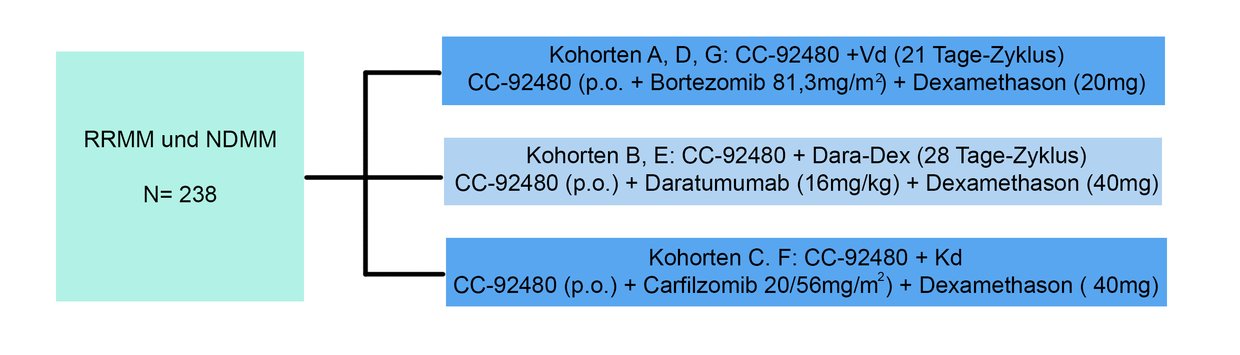
Die Studie wird randomisiert ausgeführt und die Patienten in 3 Gruppen eingeteilt, die neben dem CC-92480 unterschiedliche Zweier-Kombinationen enthalten, die gegeneinander getestet werden. Die Kohorten haben unterschiedliche Einschlusskriterien.
Ein- und Ausschlusskriterien:
Einschlusskriterien:
- Alter ≥ 18 Jahre alt und ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) mit 0, 1 oder 2 Punkten.
- Patienten mit rezidiviertem oder refraktäremMultiplen Myelom müssen eine messbare Krankheit haben und ihr Krankheitsverlauf während oder nach ihrer letzten Myelomtherapie muss dokumentiert sein.
- Bei neu diagnostizierten Patienten muss die Diagnose eines zuvor unbehandelten symptomatischen Multiplen Myeloms dokumentiert sein.
- Frauen im gebärfähigen Alter und männliche Patienten müssen mit dem Schwangerschaftsverhütungsplan einverstanden sein.
Ausschlusskriterien:
- Signifikante medizinische Erkrankung, auffällige Laborwerte oder eine psychiatrische Krankheit, die an der Teilnahme an der Studie hindert.
- Patient ist nicht in der Lage oder nicht bereit, sich der laut Prüfplan vorgeschriebenen Prophylaxe einer Thromboembolie zu unterziehen.
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt

